Exercice 2 : Exploitation de l'équation de réaction. Niveau 2
On considère maintenant la combustion de 100000 molécules de méthane en présence d'un volume d'air contenant 250000 molécules de dioxygène.
Complète le tableau ci-dessous en indiquant le nombre de molécules des réactifs 1 et 2 et des produits 1 et 2 présents à l'état final (lorsque la réaction de combustion s'arrête). Vérifie ensuite tes réponses en cliquant sur l'icône "calculer le score" du bandeau en haut de page :
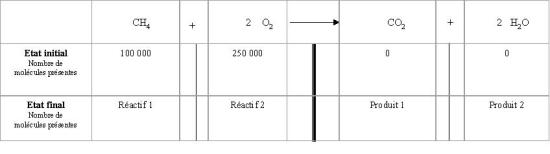
Les nombres stœchiométriques nous indiquent qu'une molécule de méthane réagit avec deux molécules de dioxygène, soit le double, 100000 molécules de méthane réagissent donc avec 2x100000 = 200000 molécules de dioxygène. En fin de combustion, toutes les molécules de méthane auront réagi et disparu mais seules 200000 molécules de dioxygène sur les 250000 initialement présentes auront réagi et disparu, il reste donc 250000 - 200000 = 50000 molécules de dioxygène. Le dioxygène est lr réactif en excès.
